关节炎的低剂量放射治疗
一、关节炎的发生机制
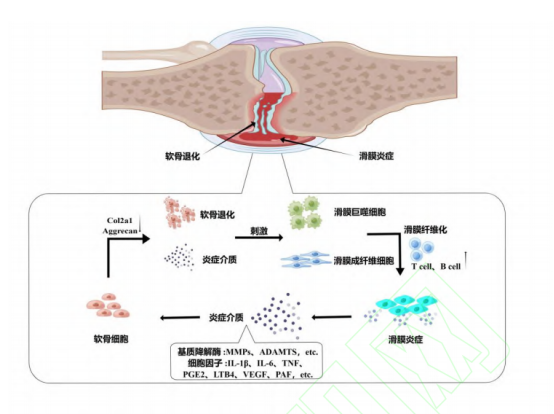
二、关节炎的的病理、危险因素、临床表现及治疗
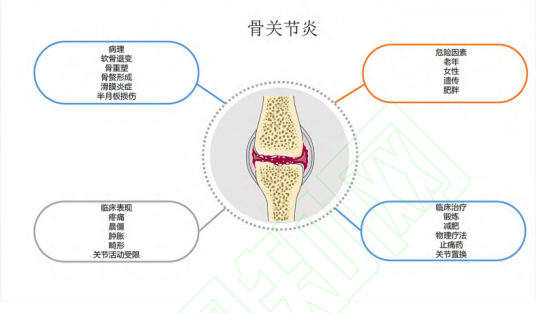
三、什么是低剂量放射(low dose radiation therapy,LDRT)?
目前,临床治疗骨关节炎疼痛的方式包括运动疗法、理疗、非甾体类抗炎药和关节内注射等,但并不能提供令人满意的止疼的效果,且长期服用药物具有潜在风险。LDRT 是一种有效的替代疗法,在关节疾病中具有缓解疼痛的作用。研究表明,LDRT 可以显著缓解疼痛水平,疼痛减轻持续长达 6 个月,甚至长达 1 年[54]。但也有报道称 LDRT 对 OA 无显著疗 效,在手部骨关节炎患者中,经低剂量放射治疗 6 个月后,有 28%的患者对治疗有反应,假手术组中有 31%的患者对治疗有反应。治疗 12 个月时,两组对治疗产生反应的患者概率分别为 31%和 27%。目前 LDRT 在德国被广泛应用于良性疾病的治疗中,良性疾病占每年接受治疗的所有患者的 1/3 以上,超过 10 000 例 OA 患者接受 LDRT,以缓解疼痛改善关节活动能力。
四、低剂量放射治疗参考方案是什么?
德国放射肿瘤学会(DEGRO)发布了对于 LDRT 治疗 OA 的建议,髋关节和膝 关节的剂量建议为 0.5 ~ 1 Gy/关节,总剂量为 3 ~ 6 Gy,给予 2 ~ 3 次/周治疗。
低剂量放射治疗膝骨关节炎的机制是什么?
1 低剂量放射治疗抑制炎症反应
放射治疗(radiation therapy, RT)多应用于癌症的治疗,高剂量放疗诱导促炎细胞因子的产生,促进照射组织中的炎症反应,相反低剂量放射治疗(low dose radiation therapy,LDRT)调节炎症反应,产生抗炎作用。LDRT 多年来已在若干国家用于治疗急慢性炎症性疾病 和疼痛性退行性疾病。 巨噬细胞经照射后诱导型一氧化氮合酶(iNOS)的表达降低、活性氧(ROS)的释放和 超氧化物的产生受抑制。LDRT 通过抑制 iNOS 从而降低一氧化氮(NO)的浓度,ROS 和 NO 浓度的降低有助于 LDRT 的局部治疗效果,减轻放疗对正常组织细胞的损伤]。此外, LDRT 还通过巨噬细胞极化调节炎症级联反应。最近的研究表明,LDRT 驱动巨噬细胞向 M2 抗炎表型分化,并诱导抗炎细胞因子微环境的产生。 此外,LDRT 可以抑制白细胞中 促炎细胞因子的产生,减少其募集和黏附,下调细胞黏附分子如选择素、细胞间黏附分子 (ICAM)和血管内皮细胞黏附分子(VCAM)的表达水平。因此,LDRT 调节内皮细胞,增加抗炎细胞因子,减缓炎症反应。另一项研究表明,低剂量 X 射线照射(0.3 ~ 0.7 Gy) 可刺激内皮细胞产生大量 TGF-β1,使内皮细胞对外周血单个核细胞(PBMC)的黏附下调, 有助于 LDRT 的抗炎作用。
2 LDRT 缓解 OA 疼痛的临床研究
关节软骨退行性变是 OA 的典型特征,但其不是引起关节疼痛的原因,因其是一种非神 经血管组织。然而,软骨下骨、骨膜、韧带和关节囊神经支配丰富,含有神经末梢。疼痛 的机制目前尚不清晰,可能是由伤害感受器刺激和疼痛传递神经元的共同作用,通过外周和 中枢神经系统以复杂的方式调节。TNF-α、IL-1β等炎症细胞因子可以刺激神经末梢,增加 疼痛的感觉和程度。NGF、BDNF 等神经生长因子可以调节神经元的功能,神经元活动异常 引起疼痛。神经致敏是 OA 患者疼痛的主要特征,疼痛刺激可以导致中枢神经系统中的放电 阈值降低,从而引起痛觉敏化和疼痛记忆。免疫和神经系统之间的双向相互作用被认为是 慢性疼痛的主要病理机制
3 LDRT 缓解 OA 的机制研究
目前,许多临床前研究都集中在 LDRT 的炎症调节作用上,LDRT 可以在刺激免疫细胞 释放正常细胞因子等活性分子的同时,降低炎症介质的表达和升高抗炎细胞因子,从而缓解疼痛和炎症,这一点在体内体外实验中都得到了验证。
在 K/BxN 小鼠模型(一种关节炎小鼠模型)上进行的一项研究显示,局部单剂量 0.5 Gy会改变骨髓中的免疫细胞亚群,这包括从炎性 CD8+ T 细胞向 CD4+ T 细胞的转变,以及树 突状细胞(DC 细胞)的显著减少。血清细胞因子也发生改变,抗炎细胞因子 IL-4 显著升高,促炎细胞因子 IL-17A 显著降低。 hTNF-αtg 小鼠经过 LDRT 后关节炎症状减轻,炎症 和侵蚀面积显著减少,破骨细胞和中性粒细胞减少,促炎性细胞因子 IL-6 减少。此外, 低于 1 Gy 的辐射剂量使巨噬细胞极化为抗炎 M2 表型,而较高剂量则有利于促炎 M1 表型 。如前所述,OA 的病理症状之一是滑膜中巨噬细胞的浸润,以及巨噬细胞 M1 的极化。因此,LDRT 缓解 OA 的机制有可能是辐照使滑膜中浸润的巨噬细胞向 M2 的转化。
新的一项研究表明,LDRT 可以通过调节线粒体的生长分化因子 15(GDF15)发挥抗炎 作用,从而缓解 OA 进展。同样他们也发现,0.25~1 Gy 的辐照剂量降低了促炎因子 MMP- 13 和 ADAMTS5 的表达,并增加了 IL -1β诱导的炎性软骨细胞中 Col2a1 的表达[59]。此外,0.5 Gy 和 1 Gy 剂量分别照射 OA 大鼠模型后,OARSI 评分显著降低。同样,本课题组使用X 射线低剂量照射 IL-1β诱导的大鼠炎症软骨细胞发现,1 Gy 以内的剂量可以促进 Col2a1和 aggrecan 的表达,降低 MMP-13 和 ADAMTS5 的表达。我们在动物实验中也发现,LDRT有缓解 OA 的作用,0.5 Gy×5 次照射 OA 大鼠模型后,滑膜中 CCL2、IL-1β 及 IFN-β1 等炎症因子降低,脊髓中 CCL2、CXCL1、IL-1β和 IFN-β1 等炎症因子减少,软骨的损伤程度也得到缓解。此外还观察到,在热板测痛实验中,OA 大鼠模型在 0.5 Gy×5 次照射后,运动 能力得到改善,爪子收缩阈值升高。
五、低剂量放射治疗的不良反应:
1.急性反应:LDRT 最大限度地减少了对周围健康组织的损伤,使患者能够耐受更频繁和更长时间的放疗。此外,与常规放疗相比,LDRT 的不良反应较少,如治疗期间关节处皮肤发红、干燥 或瘙痒,对周围软组织如肌肉、肌腱和韧带的影响最小。另一方面,厌食、恶心、呕吐和脱 发等不良反应明显减少,从而提高了患者的生活质量。由于照射剂量极低,LDRT 一般很少引起严重的急性放射反应。即使发生反应,症状也较轻,不需要进一步干预治疗
2.致癌的风险: 另一个值得考虑的问题是 LDRT 的致癌风险。目前,还不能确定 LDRT 是否能够增加癌症的风险,需要从基础研究和临床两个方面进 行大量的更深入的研究,以期取得明确的结论。由于 OA 发生在关节部位,远离代谢旺盛的组织和紧要器官,因此 LDRT 治疗 OA 引发恶性肿瘤的风险在理论上较低,但是仍然需要在今后的临床实践中,寻找进一步减少照射剂量和分次的最佳方案,降低肿瘤发生风险。
六、低剂量放射治疗治疗 膝骨关节炎的展望
现有的研究表明,LDRT 对于 OA 的治疗效果是积极的,可以缓解患者的疼痛、减轻炎症和改善生活质量,安全性较高并未出现严重的不良反应和并发症。目前在 OA 的治疗中,LDRT 并没有引起临床医生的关注,仅有少部分国家使用 LDRT 治疗 OA。后期将有不同类型的射线,包括为加速器产生的 X 射线和质子重离子射线,均有可能成为膝骨关节炎治疗的良好替代方案。
摘录自:马国榕,杨永泽,孟欣,高玉婷,李树直,郭洪章,金晓东.低剂量放疗缓 解骨关节炎[J/OL].生物化学与生物物理进展.https://doi.org/10.16476/j.pibb.2023.0432
